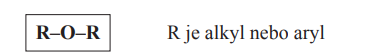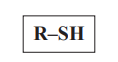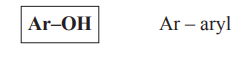8) Hydroxysloučeniny
Created by Martin Krejzek
#Maturita

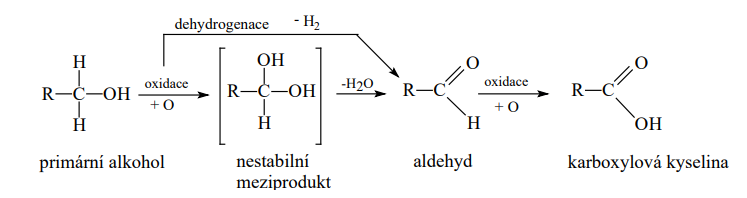
Primární alkoholy
- Se oxidují na aldehydy
- Mohou být dále oxidovány na karboxylové kyseliny účinkem KMnO4
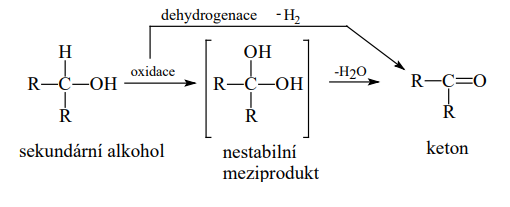
Sekundární alkoholy
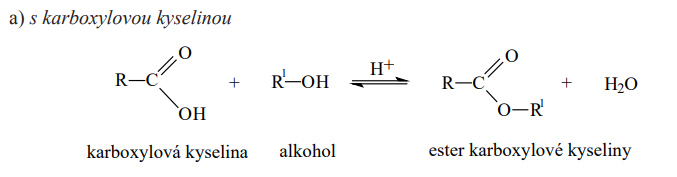
Esterifikace
- Alkohol reaguje s kyselinou za vzniku esteru a vody
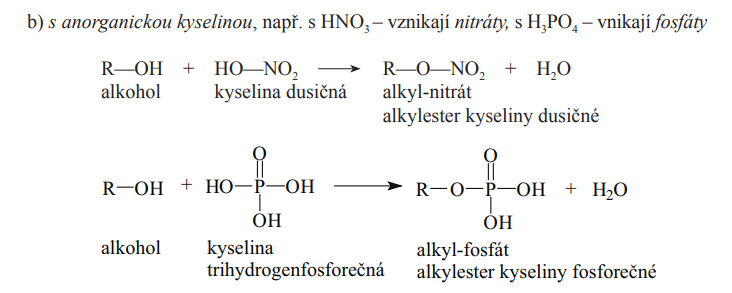
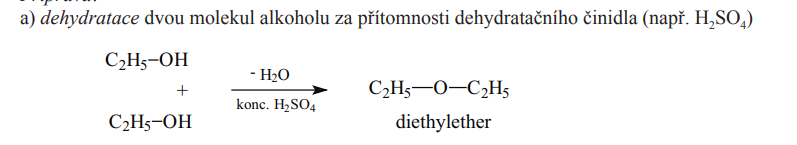
Dehydratace
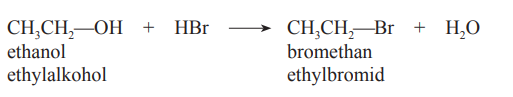
Nukleofilní substituce
- Za přítomnosti OH- skupiny
Ethanol



Dehydratací
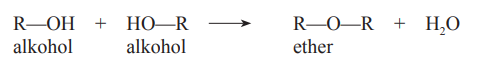
- Dvou molekul alkoholu vznikají ethery
Terciální alkoholy
- Se neoxidují
- Nemají žádný atom vodíku na uhlíku, který nese hydroxyskupinu
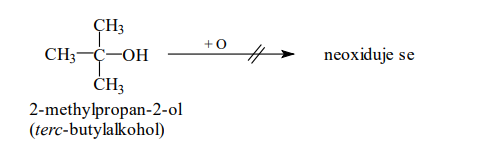
Adice
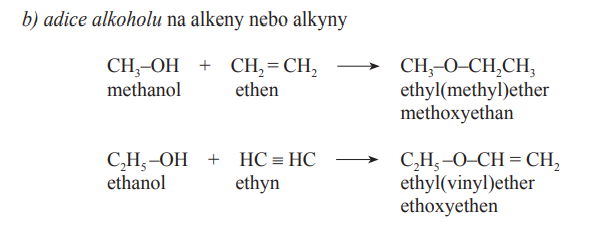
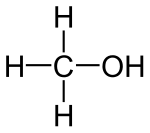
Methanol
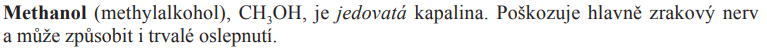
Příklady
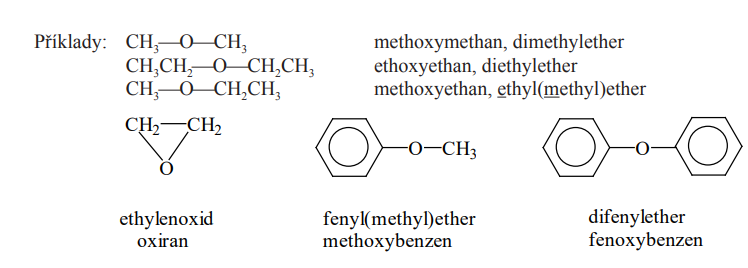

Nomenklatura

Chemické vlastnosti
Glycelor


Procvičení

Chemické vlastnosti
- Vazba kyslík - vodík je polární a proto má vodík v alkoholech slabě kyselý charakter
- Kyselý vodík, protože se mu tak říká
- Jinak je odštěpitelný kvůli polární vazbě
- Jsou to slabší kyseliny - odštěpují vodík => a podléhají hydrolýze pouze ve formě alkalického kovu
- Mohou vznikat soli sreakcí s hydroxidem ale pouze s alkalyvckým zásaditým kovem
Fyzikální vlastnosti
- Těkavé a hořlavé látky
- Mají mnohem nižší bod varu než alkoholy
- Nevznikají vodíkové můstky
- Nemísí se s vodou protože jsou nepolární
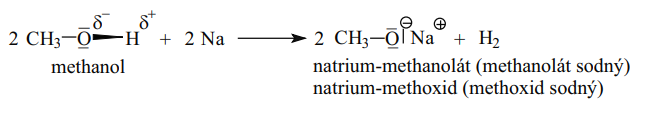
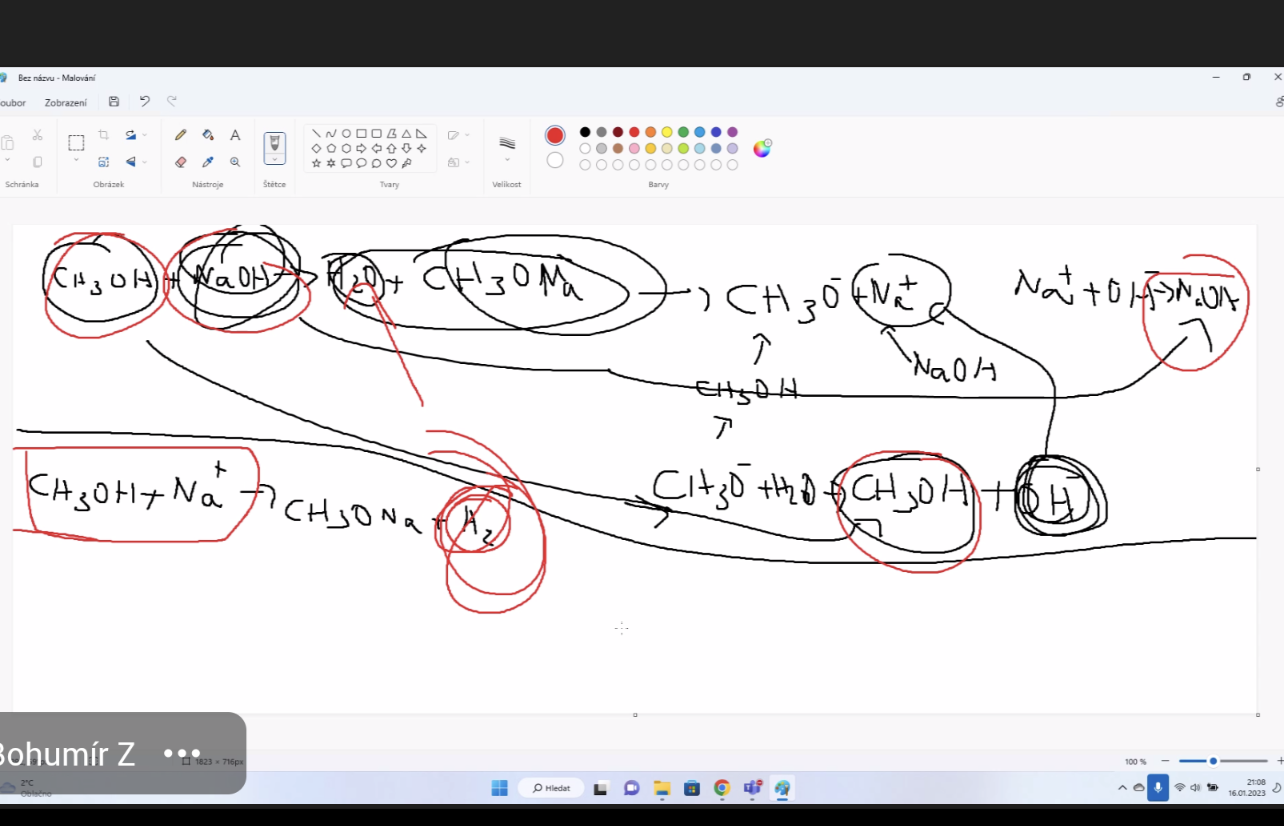
Soli alkoholů = alkoholáty
- Za přítomnosti alkalického kovu (zásady!) tvoří alkoholy alkoholáty
- Nesmí vznikat hydroxidy ale kovy
- Kdyby vznikal hydroxid, vznikla by voda a nastala by hydrolýza
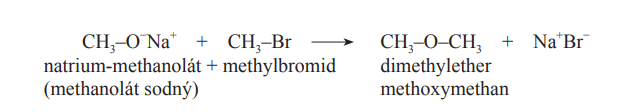
Ethery
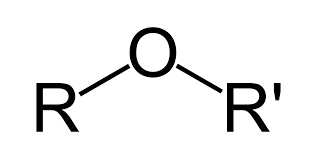
- Sloučeniny, ve kterých jsou na atom kyslíku vázány 2 uhlovodíkové substituenty
- Obecný vzorec:
Procvičení

Fyzikální vlastnosti
- Vytváří vodíkové můstky
- => VBV
- Polarita se určuje na základě elektronegativity

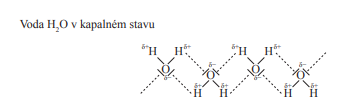
2. S délkou uhlovodíkového řetězce klesá rozpustnost alkoholů ve vodě (zvyšuje se podíl nepolární části)
8) Hydroxysloučeniny
- Sloučeniny kyslíku s OH- skupinou
Diethylether

Alkoholy

- Jsou sloučeniny, které obsahují v molekule jednu nebo více hydroxyskupin, které nejsou vázané na aromatický kruh
- Vznikají náhradou vodíku v molekule uhlovodíku skupinou OH-
Nomenklatura
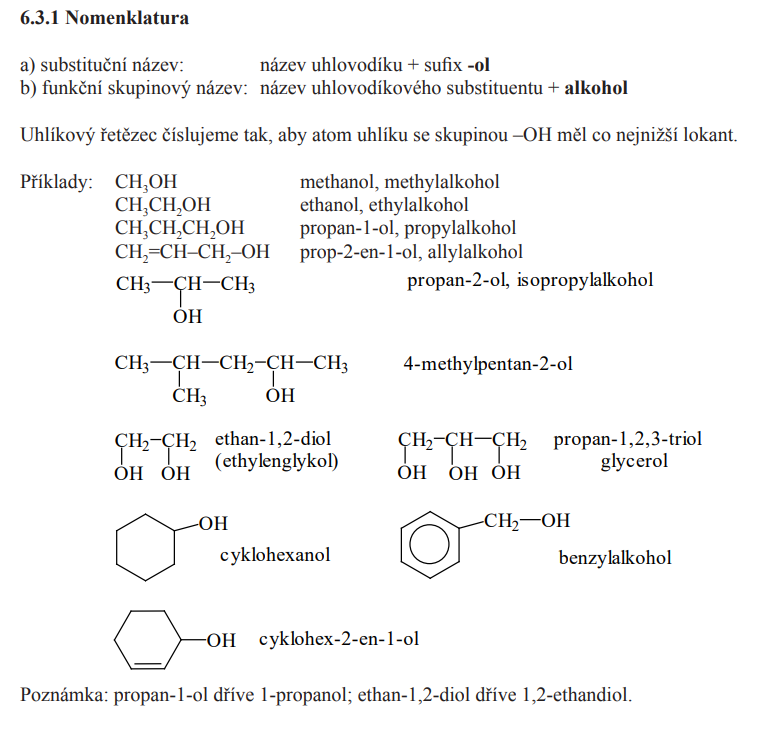
Procvičení

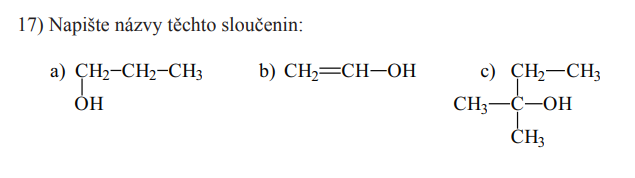
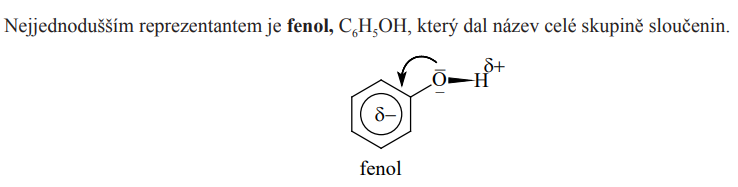
Jednosytné fenoly
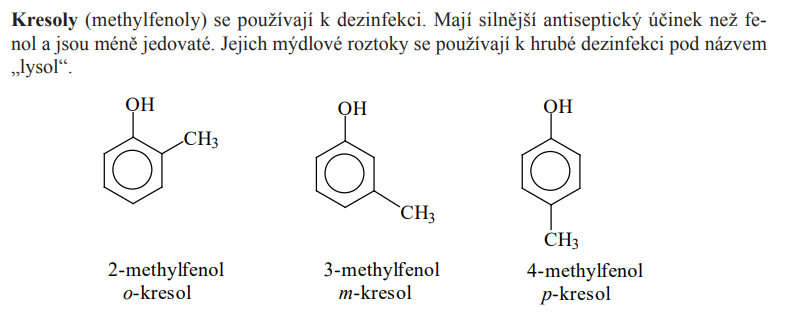
Thioly

- Jsou látky vzniklé náhradou kyslíku atomem síry
- Obecný vzorec:
- Příklady:
Terciální alkoholy
- Hydroxyskupina je na terciálním uhlíku (uhlík se 3 R)
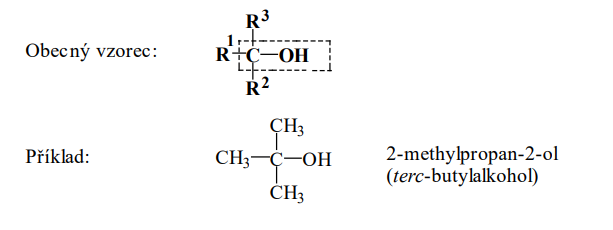
Chemické vlastnosti
- Velice nepříjemný zápach, mnohem nepříjemnější než sirovodík
Fenoly
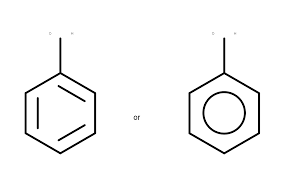
- Fenoly jsou sloučeniny, ve kterých se jedna nebo více hydroxyskupin váže na aromatický kruh
- Mají aromatické jádro
- Obecný vzorec:
- Příklad:
Sekundární alkoholy
- Hydroskupina je na sekundárním uhlíku (uhlík se 2 R)
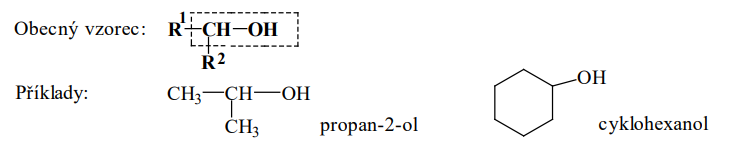
Primární alkoholy
- Hydroxyskupina je na primárním uhlíku (uhlík s jedním substituentem R)
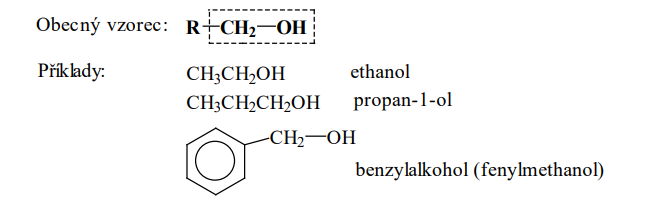
Fyzikální vlastnosti
- Nižší BV
- Nevytvářejí vodíkové můstky
Chemické vlastnosti
- Jsou podobné jako u alkoholů
- Jsou to silnější kyseliny
- Soli = fenoláty, mohou vznikat reakcí s hydroxidy
- Vytváří Se
Oxidace
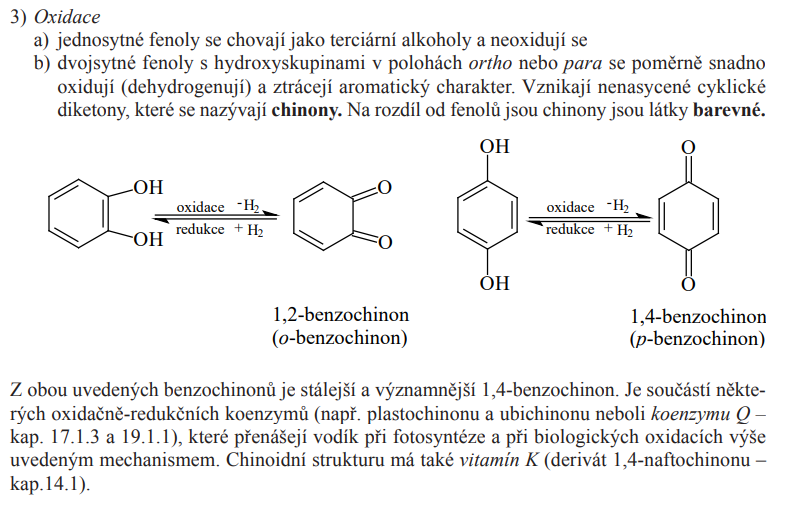
Fyzikální vlastnosti
- Malá rozpustnost ve vodě
- Čím více OH, tím jsou více rozpustnější
Trojsytné fenoly
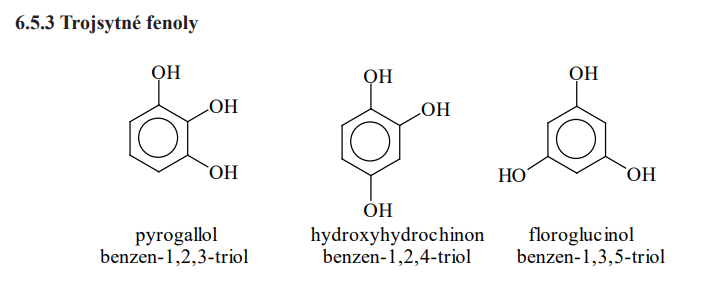
Soli > fenoláty
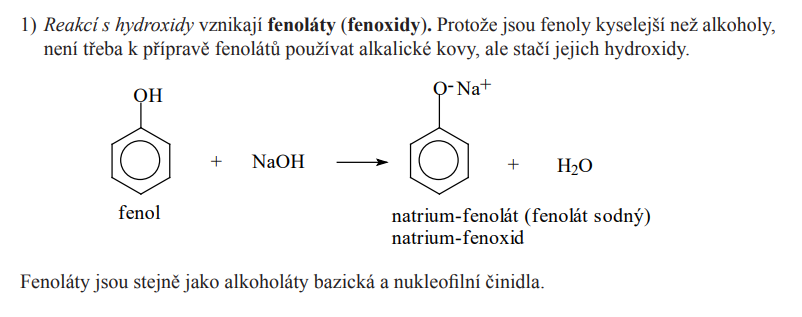
- Mohou reagovat s hydroxidy
- Jsou to silnější alkoholy
- Nedochází tím potom k hydrolýze
Esterifikace
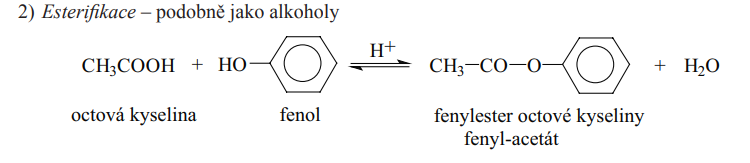
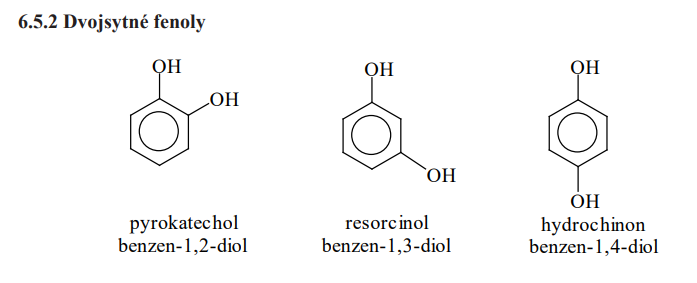
Dvojsytné fenoly
Rozdělení alkoholů
Vodíkové můstky
- Vyskytují se u sloučenin vodíku s prvkem o vysoké elektornegativitě (F, O, N)
- Atom vodíku jedné molekuly vytváří slabou vazbu s elektronegativnějším prvkem
- Elektornegativnjší prvek si elektrony přitahuje (má schopnost přitahovat ne sebe elktorny) a získává parciální záporný náboj, vodík má kladný protože na sebe nepřitahuje elektrony
- Způsobují vysoký bod varu
- Neurčuje se POLARITA!
- Když jsou nepolární, tak proč by se určovaly póly…
Významné látky
Reakce
Oxidace (dehydrogenace)
Chemické reakce
Významné ethery
Příprava etehrů