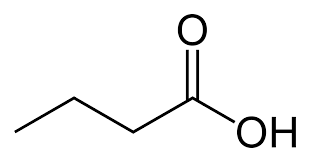
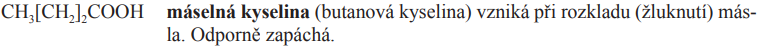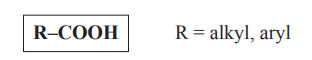12) Karboxylové kyseliny
Created by Martin Krejzek

Karboxylové kyseliny
- Jsou kyslíkaté deriváty uhlovodíků se svojí funkční skupinou COOH
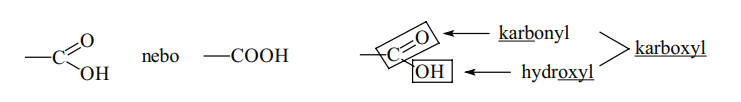
- Vzniklo spojením 2 funkčních skupin - spojením hydroxylovové skupiny (OH) a karbonylové skupiny (O)
Názvosloví
Triviální
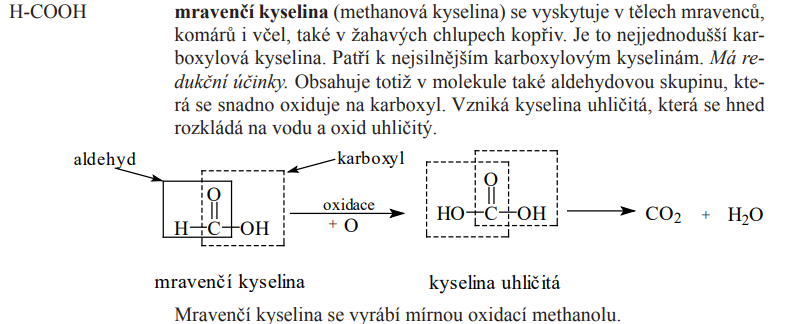
Kys. mravenčí
Kys. šťavelová
Systematické
- Tvořen z kyseliny + název uhlovodíku + koncovka - ová
- Vyjímka:
- Pokud se atom C nezpočítá do řetězce používáme koncovku karboxylová
- Př.: kys. karboxylová (C je mimo)
Chemické vlastnosti
- Proton karboxylové kyseliny je relativně kyselý
- Vazby mezi uhlíkem a kyslíkem jsou rovnocenné
- Elektrický náboj je delokalizován
Klasifikace COOH
Dle sytnosti
Jednosytné
Kyselina octová

Kys. mravenční
Vícesytné
Kys. šťavelová
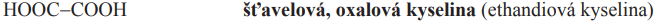
Dle uhlovodíkového zbytku
Nasycené
Kys. máselná
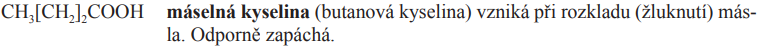
Nenasycené
Kys. olejová
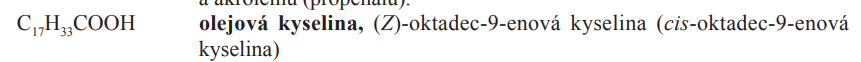
Kys. propenová
Aromatické
Kys. benzoová

Radikálová halogenace (chlorace, bromace)
Typ mechanismu: Řetězová radikálová substituce.
Fáze:
- Iniciace: Homolytické štěpení vazby (např. Cl–Cl → 2 Cl·) generuje volné radikály. Vyžaduje teplo nebo UV záření.
- Propagace: Radikál (např. Cl·) odebírá vodík z alkanu za vzniku alkylového radikálu (R·) a HCl. Alkylový radikál následně reaguje s molekulou halogenu (X₂) za vzniku alkylhalogenidu (RX) a nového halogenového radikálu (X·), který pokračuje v řetězci.
- Terminace: Spojení dvou radikálů (např. R· + R· → R–R, X· + X· → X₂, R· + X· → RX) ukončuje řetězovou reakci.
Klíčové meziprodukty: Volné radikály (alkylradikály, halogenové radikály). Jejich stabilita určuje regioselektivitu (3° > 2° > 1°).
1. Reakce SN2 (nukleofilní bimolekulární substituce)
- Mechanismus: Probíhá v jednom kroku [13] [14]. Nukleofil napadá halogenalkan z opačné strany odstupující skupiny, což vede k inverzi konfigurace (Waldenova inverze) [15]. Rychlost reakce závisí na koncentraci nukleofilu [16].
- Struktura substrátu: Nejrychlejší pro stericky nebráněné halogenalkany (methyl a primární), reaktivita klesá od methyl > primární > sekundární > neopentyl > terciární [17]. Vinyl a arylhalogenidy SN2 reakce nepodléhají [18].
- Stereochemie: 100% inverze konfigurace [19].
- Nukleofil: Rychlost reakce závisí na koncentraci nukleofilu; upřednostňuje se, je-li nukleofil anion [20]. Vyžaduje silný nukleofil (obvykle aniontový) [21].
- Odstupující skupina: X- nebo -OSO₂R [22].
- Rozpouštědlo: Rychlost reakce je málo ovlivněna polaritou rozpouštědla [23]. Upřednostňuje polární aprotická rozpouštědla (např. DMF, DMSO) [24].
Nitrace a sulfochlorace
- Nitrace: Probíhá za vysokých teplot (přibližně 430–450 °C). Předpokládá se radikálový mechanismus, při němž radikál NO₂ (generovaný například z HNO₃) odebírá vodík z alkanu a vzniklý alkylový radikál reaguje s dalším NO₂.
- Sulfochlorace: Reakce SO₂ a Cl₂ za UV záření. Předpokládá se řetězová radikálová reakce, při níž vznikají alkylsulfonylradikály (–SO₂·), jež jsou stabilizovány vazbami S=O.
1. Elektrofilní aromatická substituce (EAS)
- Podpora: Skupiny dodávající elektrony [1].
- Mechanismus: Stabilizuje karbokationtový meziprodukt [2].
- Účinek skupin odvádějících elektrony: Dezaktivuje reakci [3].
- Výsledek: Výměna atomu vodíku na kruhu [4].
Halogenace (Cl₂, Br₂)
Typ mechanismu: Elektrofilní adice s cyklickým haloniovým iontem.
Fáze: Alken napadá molekulu halogenu (X₂), čímž vzniká cyklický bromoniový (nebo chloroniový) ion. Nukleofil (X⁻) následně napadá tento ion z opačné strany (zádem), což vede ke striktní anti adici a vzniku vicinálního dihalogenidu.
Klíčové meziprodukty: Cyklický haloniový ion (bromoniový, chloroniový).
2. Nukleofilní aromatická substituce (NAS)
- Podpora: Skupiny odvádějící elektrony [5].
- Mechanismus: Stabilizuje intermediární karbanion (doslovná formulace z dokumentu) [6].
- Účinek skupin odvádějících elektrony: Aktivuje reakci [7].
- Výsledek: Výměna odstupující skupiny [8].
Hydratace (adice vody)
- Kyselinou katalyzovaná hydratace: Typ mechanismu: Elektrofilní adice s karbokationtovým meziproduktem, reverzibilní. Fáze: Podobně jako adice HX, avšak H⁺ je katalyzátor. Nejprve adice H⁺ za vzniku karbokationtu, následně atak vody (H₂O) jako nukleofilu. Posledním krokem je deprotonace vázané vody za vzniku alkoholu a regenerace H⁺. Klíčové meziprodukty: Karbokationty. Možné přesmyky.
Oxymerkurace–demerkurace: Typ mechanismu: Adice bez volného karbokationtu. Fáze: Alken reaguje s Hg(OAc)₂ za vzniku cyklického merkuroniového iontu. Ten je následně atakován molekulou vody (nukleofil) z vnější strany (anti adice) na více substituovaném uhlíku. Poté následují deprotonace a reduktivní odstranění rtuti pomocí NaBH₄. Klíčové meziprodukty: Cyklický merkuroniový ion. Bez přesmyků.
Hydroborace–oxidace: Typ mechanismu: Koncertovaná syn-adice BH₃, následovaná oxidací. Fáze: BH₃ (nebo jeho deriváty) se aduje na dvojnou vazbu v koncertovaném syn-mechanismu (H a BH₂ se přidají současně na tutéž stranu) s anti-Markovnikovovou regioselektivitou (B se váže na méně substituovaný uhlík). Následná oxidace s H₂O₂/NaOH nahradí B skupinou –OH se zachováním stereochemie (syn adice H a OH). Klíčové meziprodukty: Organoborany.
Krakování (termální)
Typ mechanismu: Radikálové štěpení vazeb.
Popis: Dlouhé uhlovodíkové řetězce jsou při vysokých teplotách homolyticky štěpeny (vazby C–C i C–H), což vede ke vzniku mnoha radikálových fragmentů. Tyto radikály dále reagují (štěpení, rekombinace, abstrakce vodíku) za vzniku kratších alkanů a alkenů.
1. Alkany: Reakce probíhající radikálovými mechanismy
Alkany jsou za normálních podmínek poměrně nereaktivní. Jejich klíčové reakce jsou obvykle vyvolány vysokou energií (teplem, UV zářením) a probíhají cestou volných radikálů.
Tvorba halohydrinů
Typ mechanismu: Modifikovaná halogenace s nukleofilním atakem vody.
Fáze: Vznik cyklického haloniového iontu probíhá stejně. V přítomnosti vody (H₂O) jako rozpouštědla voda (silnější nukleofil než X⁻) atakuje haloniový ion. Atak probíhá na více substituovaném uhlíku haloniového iontu (kvůli jeho částečnému karbokationtovému charakteru) a opět z opačné strany (anti adice). Poté následuje deprotonace vázané vody.
Klíčové meziprodukty: Cyklický haloniový ion.
Aromatické substituční reakce
gfdgd
3. Eliminace-adice (přes benzyn)
- Mechanismus: Zahrnuje přítomnost velmi silné báze (např. amid sodný) [9]. Nemusí nutně vyžadovat skupiny odvádějící elektrony [10].
- Regioselektivita: Nukleofil vstupuje nejen na uhlíkový atom, kde byl původně navázán halogen, ale také na sousední uhlíkové atomy, což vede ke směsi izomerních produktů [11].
- Průmyslová aplikace: Používá se při průmyslové výrobě fenolu, za použití zředěného vodného roztoku hydroxidu sodného při 340 °C a 18 MPa [12].
2. Reakce SN1 (nukleofilní monomolekulární substituce)
- Mechanismus: Probíhá ve dvou krocích [25]. Rychlost SN1 reakce je určena krokem tvorby karbokationtu, a proto nezávisí na koncentraci nukleofilu [26] [27].
- Struktura substrátu: Terciární haloalkan je lepší než primární [28]. Reaktivita substrátu: 3° > 2° > 1° [29]. Allylové a benzylové typy podléhají SN1, i když jsou primární [30].
- Stereochemie: Planární, achirální karbokationtový meziprodukt vede k 50% inverzi a 50% retenci konfigurace (racemizace) [31] [32]. Kompletní racemizace je méně běžná kvůli iontovým párům [33].
- Nukleofil: Reakční rychlost nezávisí na koncentraci nukleofilu; mechanismus je pravděpodobnější s neutrálními nukleofily [34]. Typicky slabý nukleofil (např. H₂O, ROH) [35].
- Odstupující skupina: X- nebo -OSO₂R. V kyselém prostředí může být i OH dobrá odstupující skupina [36].
- Rozpouštědlo: Polární protická rozpouštědla (např. voda, alkohol) jsou nejlepší [37] [38], protože stabilizují karbokationtový meziprodukt [39]. Rychlost reakce závisí na polaritě rozpouštědla [40].
Přehled reakčních mechanismů v organické chemii I
Tento přehled se soustředí na mechanismy klíčových reakcí alkanů, alkenů, konjugovaných dienů a alkynů, jak byly popsány v přednáškách Dr. Athanasiose Markose.
2. Alkeny: Elektrofilní adiční reakce a oxidace
Dvojná vazba alkenů je bohatá na elektrony a typicky funguje jako nukleofil, který reaguje s elektrofily.
Adice HX (např. HBr)
Typ mechanismu: Elektrofilní adice s karbokationtovým meziproduktem.
Fáze:
- Elektrofilní atak: Dvojná vazba alkenu napadá H⁺ z HX, čímž vzniká stabilnější karbokationt (podle Markovnikovova pravidla – H⁺ se váže na méně substituovaný uhlík, aby vznikl stabilnější karbokationt 3°/2°).
- Nukleofilní atak: Nukleofil (X⁻) napadá karbokationt a vytváří alkylhalogenid.
Klíčové meziprodukty: Karbokationty (3° > 2° > 1°). Možné přesmyky karbokationtů.
Katalytická hydrogenace (redukce na alkany)
Typ mechanismu: Heterogenní syn-adice vodíku na povrchu kovu.
Fáze: Alken a molekula vodíku jsou adsorbovány na povrch kovu (Pd, Pt, Ni). Vazby H–H a π-vazba alkenu jsou oslabeny. Vodíkové atomy se postupně přidávají na tutéž stranu dvojné vazby (syn-adice) v koncertovaném mechanismu, čímž vzniká alkan, jenž se desorbuje z povrchu.
Klíčové meziprodukty: Žádné; reakce probíhá na katalytickém povrchu.
3. Konjugované dieny: Specifické adice a cykloadice
Konjugované dieny mají delokalizované π elektrony, což ovlivňuje jejich reaktivitu a stabilitu.
Substituční a eliminační reakce halogenalkanů
4. Alkyny: Adice na trojnou vazbu a redukce
Trojná vazba alkynů je tvořena jednou σ a dvěma π vazbami, což jí propůjčuje vysokou elektronovou hustotu a schopnost reagovat s elektrofily.
3. Reakce E2 (bimolekulární eliminace)
- Mechanismus: Probíhá v jednom kroku bez tvorby meziproduktů [41]. Obě částice se odštěpují současně [42]. Zahrnuje silnou bázi působící na halogenalkan [43].
- Stereoselektivita: Přednostně je eliminován proton, který je anti vzhledem k odstupující skupině (antiperiplanární konformace) [44].
- Substrát: 1°, 2° nebo 3°. Pro 1° je nezbytná silná a stericky bráněná báze [45].
- Typ báze: Vyžaduje silnou bázi (např. NaOR, NaNR₂) [46].
- Odstupující skupina: X- nebo -OSO₂R [47].
- Rozpouštědlo: Polární protické nebo aprotické [48].
Stereoselektivní redukce
- Hydrogenace na cis-alkeny (Lindlarův katalyzátor): Typ mechanismu: Heterogenní syn-adice vodíku na „otráveném" katalyzátoru. Fáze: Obdobně jako hydrogenace alkenů, avšak „otrávený" katalyzátor (např. Pd/BaCO₃ s chinolinem) snižuje jeho aktivitu natolik, že redukuje pouze trojnou vazbu na dvojnou, nikoli na jednoduchou. Vodíkové atomy se adují syn (z jedné strany), čímž vzniká cis-alken. Klíčové meziprodukty: Žádné; reakce probíhá na katalytickém povrchu.
Redukce na trans-alkeny (Birchova redukce, Na/NH₃ (kapal.)): (Text originálu byl zkrácen; tato část bude doplněna po předložení úplného zdroje.)
Dihydroxylace (tvorba diolů)
Syn-dihydroxylace (OsO₄ nebo studený KMnO₄): Typ mechanismu: Koncertovaná syn-adice s cyklickým meziproduktem. Fáze: Alken reaguje s OsO₄ v koncertovaném syn-mechanismu za vzniku cyklického osmičnanového esteru. Následná hydrolytická štěpení vazeb O–Os uvolní diol, v němž jsou obě skupiny –OH na téže straně původní dvojné vazby. Podobný, avšak méně přesně definovaný mechanismus platí i pro studený KMnO₄. Klíčové meziprodukty: Cyklický osmičnanový ester.
Anti-dihydroxylace (epoxidace + kysele katalyzované otevření): Typ mechanismu: Dvoustupňový proces s inverzí konfigurace ve druhém kroku.
Fáze: Nejprve epoxidace (viz níže) za vzniku epoxidu (syn adice kyslíku). Následně kysele katalyzované otevření epoxidu: protonace kyslíku epoxidu, nukleofilní atak vody na jeden z uhlíků epoxidu z opačné strany (anti atak) a konečná deprotonace za vzniku anti-diolu. Klíčové meziprodukty: Epoxid (cyklický ether).
Epoxidace (s peroxykyselinami, např. mCPBA)
Typ mechanismu: Koncertovaná syn-adice kyslíku.
Fáze: Atom kyslíku z peroxykyseliny se aduje na dvojnou vazbu v jednom kroku a syn-mechanismu (z jedné strany), čímž vzniká tříčlenný cyklický ether – epoxid.
Klíčové meziprodukty: Žádné stabilní meziprodukty, pouze cyklický přechodový stav.
Ozonolýza
Typ mechanismu: Dvoustupňový cykloadiční proces.
Fáze: Ozon (O₃) nejprve reaguje s alkenem v [3+2] cykloadiční reakci za vzniku primárního ozonidu (molozonidu), který je velmi nestabilní. Molozonid se následně rychle rozkládá na karbonylovou sloučeninu a karbonylový oxid. Tyto dva fragmenty se pak znovu rekombinují v obrácené [3+2] cykloadiční reakci za vzniku stabilnějšího sekundárního ozonidu. Ten je poté reduktivně štěpen (např. zinkem v CH₃COOH nebo Me₂S) na karbonylové sloučeniny (aldehydy/ketony).
Klíčové meziprodukty: Primární ozonid (molozonid), sekundární ozonid.
Diels–Alderova cykloadice
Typ mechanismu: [4+2] Koncertovaná cykloadice.
Fáze: Jde o jednostupňovou reakci (koncertovaný mechanismus), při níž se současně tvoří dvě nové σ-vazby. HOMO dienu reaguje s LUMO dienofilu (nebo naopak). Elektronové páry se přesouvají v cyklickém přechodovém stavu (šestičlenný kruh). Dien musí být v konformaci s-cis, aby mohl reagovat.
Klíčové meziprodukty: Žádné; reakce probíhá přes cyklický přechodový stav.
4. Reakce E1 (monomolekulární eliminace)
- Mechanismus: Začíná samovolným štěpením vazby C-X v halogenalkanu (podobně jako u SN1) [49]. Následně však nedojde k substituci halogenu nukleofilem, ale k odtržení H+ z přechodně vzniklého karbokationtu [50].
- Substrát: Substráty nejvhodnější pro E1 jsou zároveň nejvhodnějšími i pro SN1-reakce (vznikají směsi produktů obou těchto reakcí) [51]. Reaktivita substrátu: 3° > 2° > 1° [52]. Allylový nebo benzylový typ podléhá SN1, i když je primární [53].
- Typ báze: Obecně slabá báze (např. H₂O, ROH, H₂SO₄) [54].
- Odstupující skupina: X- nebo -OSO₂R. V kyselém prostředí může být i OH dobrá odstupující skupina [55].
- Rozpouštědlo: Polární protické [56].
- Teplota: Zvýšená teplota podporuje eliminaci [57].
lekce-11-2.pdf:
Klasifikace COOH

Elektrofilní adice (např. HBr)
Typ mechanismu: Elektrofilní adice s allylovým karbokationtovým meziproduktem rezonančně stabilizovaným.
Fáze: H⁺ se aduje na jeden z koncových uhlíků konjugovaného dienu, čímž vzniká rezonančně stabilizovaný allylový karbokationt s kladným nábojem delokalizovaným přes dva uhlíky. Nukleofil (Br⁻) může následně atakovat buď uhlík v poloze 2 (za vzniku 1,2-aduktu), nebo uhlík v poloze 4 (za vzniku 1,4-aduktu).
Klíčové meziprodukty: Rezonančně stabilizovaný allylový karbokationt. Poměr produktů (kinetická vs. termodynamická kontrola) je dán stabilitou přechodového stavu, respektive stabilitou produktu.
Hydratace
Rtuťnatá katalýza: Typ mechanismu: Elektrofilní adice s enolovým meziproduktem, následovaná tautomerizací.
Fáze: Ionty Hg²⁺ (elektrofil) se koordinují s trojnou vazbou za vzniku cyklického rtuťnatého iontu. Voda atakuje tento ion Markovnikovovým způsobem. Po deprotonaci a uvolnění rtuti vzniká enol (alkohol s dvojnou vazbou), který se rychle tautomerizuje (přesun H a π elektronů) na stabilnější keton. Klíčové meziprodukty: Enol.
Hydroborace–oxidace: Typ mechanismu: Anti-Markovnikovova adice s enolovým meziproduktem, následovaná tautomerizací. Fáze: BH₃ se aduje na trojnou vazbu s anti-Markovnikovovou regioselektivitou (B na méně substituovaný uhlík). Po oxidaci s H₂O₂/NaOH je bor nahrazen skupinou –OH. Vzniká enol, který se tautomerizuje na aldehyd. Klíčové meziprodukty: Enol.
Nomenklatura COOH




Tereftalová kyselina

Adice HX a X₂
Typ mechanismu: Elektrofilní adice (obdobně jako u alkenů, avšak s vinylovým kationtem).
Fáze: Nejprve elektrofil (H⁺ nebo X⁺ z X₂) napadá trojnou vazbu za vzniku vinylového kationtu. Ten je stabilnější, je-li kladný náboj na více substituovaném uhlíku (Markovnikovovo pravidlo). Následně nukleofil (X⁻) atakuje vinylový kationt. Je-li přítomno dostatečné množství reagentu, proces se může opakovat na nově vzniklé dvojné vazbě, čímž vznikají dihalogenidy (geminální v případě HX).
Klíčové meziprodukty: Vinylové kationty.
Procvičení


Ftalová kyselina

Chemické vlastnosti
- Ovlivněné karboxylovou skupinou
- Navázat teď fyzikálními vlastnostmi
Aromatické
12) Karboxylové kyseliny
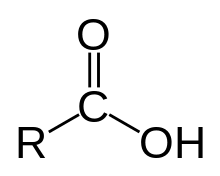
- Karboxylové kyseliny jsou sloučeniny s funkční karboxylovou skupinou krátce zvanou karboxyl
- Karboxylová funkční skupina obsahuje karbonylovou funkční skupinu, na jejíž atom uhlíku je vázána hydroxyskupina (dříve hydroxyl)
- Obecný vzorec:
Kyselina hexandiová

Nenasycené
Kyselina butandiová

Fyzikální vlastnosti
- Vytváří V.M.
- Způsobují vysoký bod varu
- Čím více COOH, tím více polární
- Neurčuje se S, A, E, N
- S délkou uhlovodíkového řetězce se rozpustnost snižuje
- Pevné i kapalné skupenství
Významné dikarboxylové kyseliny
Nasycené
Kyselina propandiová

Neutralizace
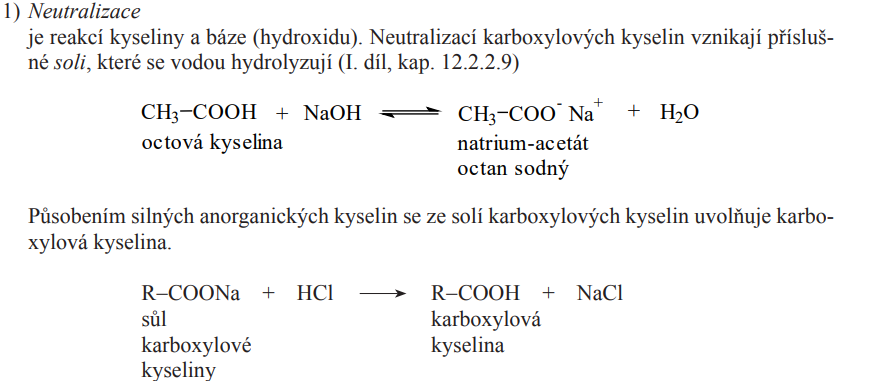
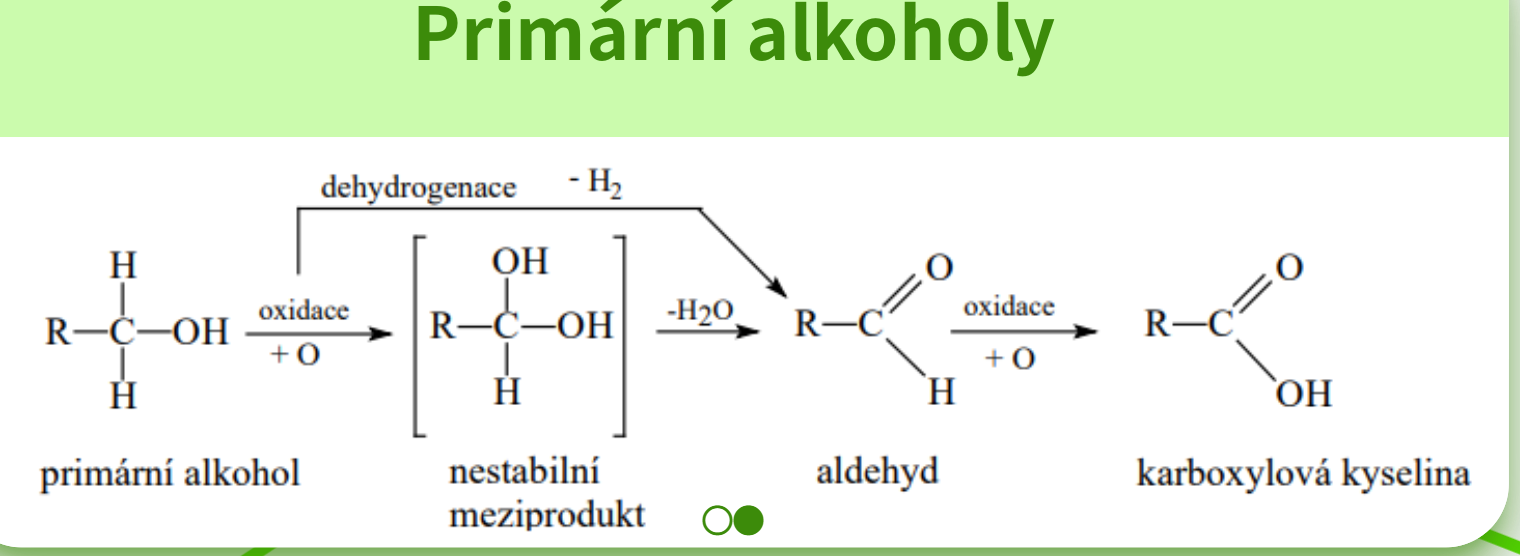
Významné monokarboxylové kyseliny
Vyšší mastné
Kyselina steraová
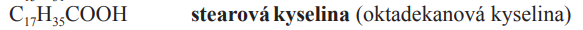
Kyselina šťavelová
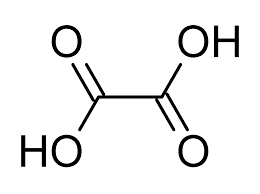
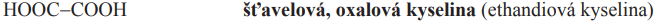
- Ve vodě rozustná bílá krystalická látka, která leptá sliznici a sráží v krvi vápenaté ionty
- Výskyz: soli v tostlinách (šťaveli, rebarboře)
- oužití: v chemické analýze
Chemické reakce
Esterifikace
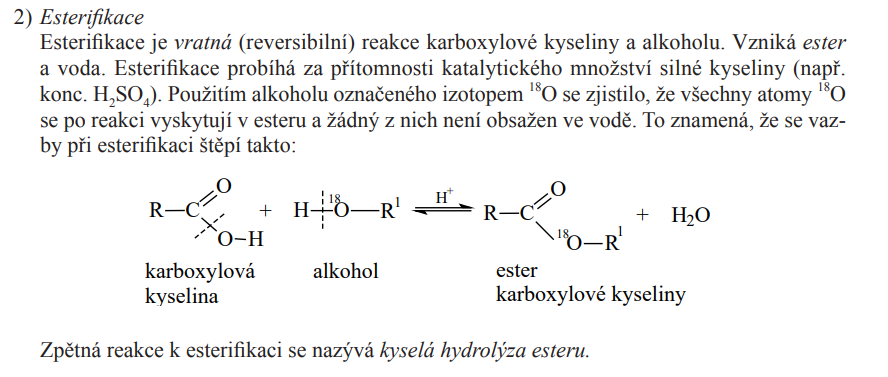
Kyselina mravenčí

- Rozkládá se pomocí konc. kys. sírové
- Konzervace potravin
Nasycené
Aromatické
Nenasycené
Kyselina palmitová
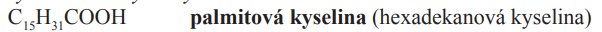
- Estery které se vykytují v tucích
- Používá se při výrobě svíček, krémů a past
Kyselina benzoová

- Ve vodě málo rozpustná látka
- Výskyt: v pryskiřici benzoe
Dekarboxylace
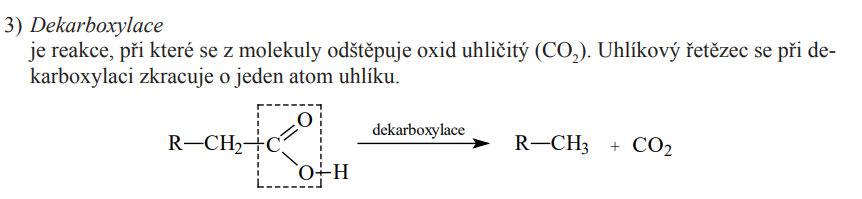
Kyselina octová
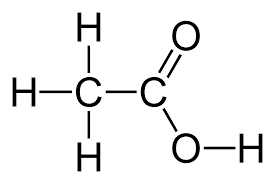

- Při 16 stupních celsia tuhne (ledová kys. octová)
- Vyrábí se oxidací acetaldehydu a vzniká voda
Kyselina olejová
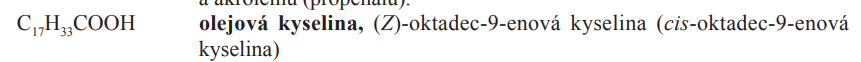
Dehydratace
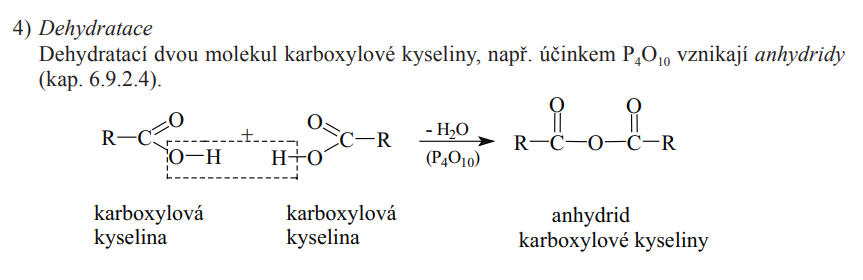
Kyselina propionová
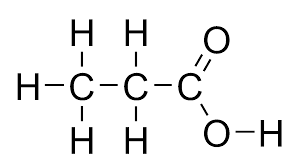

Kyselina máselná = butanová